Dott. Ignazio Madonia
Nutrizione Artificiale
Quando e Quale ?
Che cosa è la malnutrizione ?

E' lo stato di alterazione funzionale, strutturale o di sviluppo conseguente ad uno squilibrio in negativo tra fabbisogni (inalterati/aumentati) ed apporti (insufficienti).
La caratteristica clinica della malnutrizione è la riduzione di massa magra con conseguente calo ponderale. Le conseguenze correlate sono: aumentata suscettibilità alle infezioni; ritardata guarigione delle ferite; aumento del periodo di degenza; peggioramento della qualità di vita.
L’unico obiettivo della Nutrizione Artificiale (NA) è quello di trattare o prevenire lo sviluppo della malnutrizione. La NA non "cura" alcuna malattia e non modifica l‘evoluzione delle patologie. Può tuttavia essere determinante nella prevenzione dello sviluppo di complicanze (ad esempio post-chirurgiche nel paziente gravemente malnutrito), e può migliorare la qualità di vita del paziente.
La caratteristica clinica della malnutrizione è la riduzione di massa magra con conseguente calo ponderale. Le conseguenze correlate sono: aumentata suscettibilità alle infezioni; ritardata guarigione delle ferite; aumento del periodo di degenza; peggioramento della qualità di vita.
L’unico obiettivo della Nutrizione Artificiale (NA) è quello di trattare o prevenire lo sviluppo della malnutrizione. La NA non "cura" alcuna malattia e non modifica l‘evoluzione delle patologie. Può tuttavia essere determinante nella prevenzione dello sviluppo di complicanze (ad esempio post-chirurgiche nel paziente gravemente malnutrito), e può migliorare la qualità di vita del paziente.
Che cosa è la nutrizione artificiale ?

E' la somministrazione di macronutrienti (proteine, carboidrati, lipidi) e micronutrienti (elettroliti, vitamine e oligoelementi) attraverso una via artificiale al fine di coprire in parte o del tutto i fabbisogni nutrizionali del paziente. Le indicazioni ad una NA sono limitate a quelle situazioni in cui la malnutrizione è già sviluppata e non si è in grado di risolverla con un apporto alimentare corretto; dove sussistano talune condizioni che precludano un'adeguata alimentazione per via naturale per periodi > 7 – 10 giorni; o quando lo stato di malnutrizione è tale da inficiare l'evoluzione della patologia clinica di base.
Come Nutrizione Artificiale (NA), si intende solo la somministrazione di nutrienti attraverso vie artificiali, e cioè sonde o stomie per la enterale (NE), accessi venosi di vario tipo per la parenterale (NP).
Nutrizione enterale (NE) = infusione di miscele nutritive nella via digestiva (stomaco; digiuno) attraverso un sistema artificiale (sonda o stomia)
Nutrizione parenterale (NP) = infusione di soluzione nutrizionale in un vaso venoso, periferico o centrale (vena cava)
La NA non è esente da complicazioni, per questo motivo, la sua gestione viene affidata a personale esperto ed addestrato.
La Nutrizione Enterale è preferita rispetto alla NTP perché è più sicura ed economica ed è quella che comporta minori complicanze, inoltre ricordarsi che è sempre da preferire” la via naturale”.
La Nutrizione Enterale si riserva ai Pazienti che pur mantenendo l’integrità funzionale del tratto gastroenterico non possono assumere gli alimenti naturalmente, questa và somministrata a tutti i pazienti che:
Non Possono Mangiare
Non Devono mangiare
Non Vogliono Mangiare
Non Mangiano Abbastanza.
Per utilizzare le vie di somministrazione si fa uso di : Sondino Naso gastrico, o naso digiunale.
Un altro sistema molto in uso ed altrettanto efficace è il sistema di Gastrostomia Endoscopica Percutanea ( PEG ) .
Il Sondino naso gastrico può essere di diverso materiale : Silicone, Poliuretano, Gomma, in modo tale da permettere una permanenza poco traumatica.
La Gastrostomia endoscopica percutanea è molto in uso per i pazienti con tratto gastrointestinale integro per una nutrizione enterale superiore ad un mese, la PEG permette di infondere la miscela nutrizionale, direttamente nella cavità viscerale (stomaco o digiuno) attraverso una stomia (bocca) questo sistema rivoluzionario si sostituisce spesso al sondino poiché questo spesso è mal tollerato.
Indicazioni: le patologie che trovano più frequentemente indicazione al posizionamento di una PEG, sia perché alterano i meccanismi della deglutizione o dello stato di coscienza, sia perchè impediscono l’introduzione o la normale progressione del bolo alimentare, sono:
Malattie neurologiche: sclerosi laterale amiotrofica (SLA), Vasculopatie cerebrali, Trauma cranico, Demenza, Neoplasie cerebrali, Epilessia, Idrocefalo, Sindrome di Guillan Barrè , Ascesso cerebrale.
Malattie Neoplastiche: Cancro esofageo , Cancro gastrico, Neoplasie ORL, Cancro polmonare, Neoplasie Cerebrali.
Esistono altre malattie dove l’uso di tale metodica è opportuna, ma bisogna fare un’attenta valutazione da caso a caso.
Esistono in commercio diversi tipi di sonda, la PEG è una protesi al Silicone, Poliuretano o al Carbotano, del diametro di 10 fino a 20 CH, della lunghezza di circa 40 cm, con un Bumper (bottone ) morbito.
Le sonde in Silicone possono stare in sito fino a sei mesi; Le sonde in poliuretano fino a due anni; le sonde al Carbotano possono essere lasciate per più di tre anni.
Il posizionamento della PEG può essere effettuato con due metodiche diverse:
1) Pull-string Ponsky-Gauderer type Gastrostomy.
2) Push-over-wire Sachs-vine gastrostomy.
Queste due metodiche sono simili nella prima parte della procedura si diversificano tra loro soltanto nella parte finale del procedimento
Nutrizione Parenterale Totale: la NTP è un metodo per fornire sostanze nutritive all’organismo per via endovenosa ai pazienti che non possono assumere liquidi o alimenti per bocca.
Si effettua mediante catetere venoso centrale CVC o periferico.
Gli obiettivi della NTP sono di migliorare lo stato nutrizionale, stabilire un bilancio azotato positivo, mantenere la massa muscolare, favorire l’aumento di peso e stimolare la guarigione della ferita chirurgica.
La NTP è indicata quando il paziente ha un deficit del peso corporeo pari al 10%; non sia in grado di assumere alimenti o liquidi per bocca entro 7 giorni dall’intervento chirurgico e in situazioni di ipercatabolismo, per esempio in caso di infezioni accompagnate da febbre.
I componenti delle miscele nutrizionali, definiti “Substrati, possono essere distinti in :
· Macroelementi (acqua, glucidi, aminoacidi e lipidi)
· Microelementi (elettroliti, vitamine, farmaci);
· Oligoelementi ( sono 15 – ferro, zinco, rame, cromo, selenio, iodio, cobalto, manganese, nichel, molibdeno, fluoro, stagno, silicio, vanadio ed arsenico. N.B. i primi sette sono indispensabili all’uomo).
La modalità di somministrazione della NPT può essere : continua, o ciclica (Notturna)
In genere il trattamento viene iniziato con gradualità e continuamente.
La NPT e possibile somministrarla “a caduta” o con l’utilizzo di una pompa, questa consente un somministrazione regolare e precisa delle soluzioni secondo volumi e tempo programmati.
La somministrazione dei liquidi nutrizionali si può effettuare attraverso :
La grande maggioranza dei cateteri è oggi realizzata in:
1) Polietilene
2) Poliuretano
3) Silicone
Complicanze: queste possono insorgere subito (complicanze immediate) o dopo (compl. Tardive), le prime sono dovute alla manovra dell’impianto e possono essere:
· Puntura dell’arteria;
· Pneumotorace: causato dalla perforazione della parete toracica con ingresso dell’aria dall’esterno nella cavità pleurica (cavità virtuale)
· Embolia gassosa;
· Tachicardia ventricolare o aritmie;
· Danno del plesso brachiale;
· Emotorace;
· Idrotorace ;
· Embolia del catetere.
Le complicanze tardive, sono in genere dovute ad una non corretta gestione dei dispositivi; ( Infezioni, trombosi della vena ospitante il CVC, rotture del segmento esterno del catetere, Occlusione del CVC, ecc.
Cateterismo venoso periferico (CVP): l’accesso venoso periferico permette il collegamento tra la superficie cutanea e una vena del circolo periferico: Basilica, cefalica, Pedidia, o altre vene periferiche visibili; sono realizzati con materiale biocompatibile (Teflon, Poliuretano, Silicone) questi possono restare in loco a breve termine 3-4 giorni; o a medio termine fino a 4 settimane.
Per concludere è bene ricordare che la nutrizione parenterale deve essere sospesa gradualmente per consentire l’adattamento dell’assistito a un decremento dei livelli di glucosio.
Come Nutrizione Artificiale (NA), si intende solo la somministrazione di nutrienti attraverso vie artificiali, e cioè sonde o stomie per la enterale (NE), accessi venosi di vario tipo per la parenterale (NP).
Nutrizione enterale (NE) = infusione di miscele nutritive nella via digestiva (stomaco; digiuno) attraverso un sistema artificiale (sonda o stomia)
Nutrizione parenterale (NP) = infusione di soluzione nutrizionale in un vaso venoso, periferico o centrale (vena cava)
La NA non è esente da complicazioni, per questo motivo, la sua gestione viene affidata a personale esperto ed addestrato.
La Nutrizione Enterale è preferita rispetto alla NTP perché è più sicura ed economica ed è quella che comporta minori complicanze, inoltre ricordarsi che è sempre da preferire” la via naturale”.
La Nutrizione Enterale si riserva ai Pazienti che pur mantenendo l’integrità funzionale del tratto gastroenterico non possono assumere gli alimenti naturalmente, questa và somministrata a tutti i pazienti che:
Non Possono Mangiare
Non Devono mangiare
Non Vogliono Mangiare
Non Mangiano Abbastanza.
Per utilizzare le vie di somministrazione si fa uso di : Sondino Naso gastrico, o naso digiunale.
Un altro sistema molto in uso ed altrettanto efficace è il sistema di Gastrostomia Endoscopica Percutanea ( PEG ) .
Il Sondino naso gastrico può essere di diverso materiale : Silicone, Poliuretano, Gomma, in modo tale da permettere una permanenza poco traumatica.
La Gastrostomia endoscopica percutanea è molto in uso per i pazienti con tratto gastrointestinale integro per una nutrizione enterale superiore ad un mese, la PEG permette di infondere la miscela nutrizionale, direttamente nella cavità viscerale (stomaco o digiuno) attraverso una stomia (bocca) questo sistema rivoluzionario si sostituisce spesso al sondino poiché questo spesso è mal tollerato.
Indicazioni: le patologie che trovano più frequentemente indicazione al posizionamento di una PEG, sia perché alterano i meccanismi della deglutizione o dello stato di coscienza, sia perchè impediscono l’introduzione o la normale progressione del bolo alimentare, sono:
Malattie neurologiche: sclerosi laterale amiotrofica (SLA), Vasculopatie cerebrali, Trauma cranico, Demenza, Neoplasie cerebrali, Epilessia, Idrocefalo, Sindrome di Guillan Barrè , Ascesso cerebrale.
Malattie Neoplastiche: Cancro esofageo , Cancro gastrico, Neoplasie ORL, Cancro polmonare, Neoplasie Cerebrali.
Esistono altre malattie dove l’uso di tale metodica è opportuna, ma bisogna fare un’attenta valutazione da caso a caso.
Esistono in commercio diversi tipi di sonda, la PEG è una protesi al Silicone, Poliuretano o al Carbotano, del diametro di 10 fino a 20 CH, della lunghezza di circa 40 cm, con un Bumper (bottone ) morbito.
Le sonde in Silicone possono stare in sito fino a sei mesi; Le sonde in poliuretano fino a due anni; le sonde al Carbotano possono essere lasciate per più di tre anni.
Il posizionamento della PEG può essere effettuato con due metodiche diverse:
1) Pull-string Ponsky-Gauderer type Gastrostomy.
2) Push-over-wire Sachs-vine gastrostomy.
Queste due metodiche sono simili nella prima parte della procedura si diversificano tra loro soltanto nella parte finale del procedimento
Nutrizione Parenterale Totale: la NTP è un metodo per fornire sostanze nutritive all’organismo per via endovenosa ai pazienti che non possono assumere liquidi o alimenti per bocca.
Si effettua mediante catetere venoso centrale CVC o periferico.
Gli obiettivi della NTP sono di migliorare lo stato nutrizionale, stabilire un bilancio azotato positivo, mantenere la massa muscolare, favorire l’aumento di peso e stimolare la guarigione della ferita chirurgica.
La NTP è indicata quando il paziente ha un deficit del peso corporeo pari al 10%; non sia in grado di assumere alimenti o liquidi per bocca entro 7 giorni dall’intervento chirurgico e in situazioni di ipercatabolismo, per esempio in caso di infezioni accompagnate da febbre.
I componenti delle miscele nutrizionali, definiti “Substrati, possono essere distinti in :
· Macroelementi (acqua, glucidi, aminoacidi e lipidi)
· Microelementi (elettroliti, vitamine, farmaci);
· Oligoelementi ( sono 15 – ferro, zinco, rame, cromo, selenio, iodio, cobalto, manganese, nichel, molibdeno, fluoro, stagno, silicio, vanadio ed arsenico. N.B. i primi sette sono indispensabili all’uomo).
La modalità di somministrazione della NPT può essere : continua, o ciclica (Notturna)
In genere il trattamento viene iniziato con gradualità e continuamente.
La NPT e possibile somministrarla “a caduta” o con l’utilizzo di una pompa, questa consente un somministrazione regolare e precisa delle soluzioni secondo volumi e tempo programmati.
La somministrazione dei liquidi nutrizionali si può effettuare attraverso :
- Vena centrale: per somministrare soluzioni ad alta osmolarità, inserito nella vena giugulare o nella vena cava superiore.
- Vena periferica: per somministrare soluzioni a bassa osmolarità, inserito in vene di piccolo calibro (es. vena mediana dell’avambraccio).
La grande maggioranza dei cateteri è oggi realizzata in:
1) Polietilene
2) Poliuretano
3) Silicone
Complicanze: queste possono insorgere subito (complicanze immediate) o dopo (compl. Tardive), le prime sono dovute alla manovra dell’impianto e possono essere:
· Puntura dell’arteria;
· Pneumotorace: causato dalla perforazione della parete toracica con ingresso dell’aria dall’esterno nella cavità pleurica (cavità virtuale)
· Embolia gassosa;
· Tachicardia ventricolare o aritmie;
· Danno del plesso brachiale;
· Emotorace;
· Idrotorace ;
· Embolia del catetere.
Le complicanze tardive, sono in genere dovute ad una non corretta gestione dei dispositivi; ( Infezioni, trombosi della vena ospitante il CVC, rotture del segmento esterno del catetere, Occlusione del CVC, ecc.
Cateterismo venoso periferico (CVP): l’accesso venoso periferico permette il collegamento tra la superficie cutanea e una vena del circolo periferico: Basilica, cefalica, Pedidia, o altre vene periferiche visibili; sono realizzati con materiale biocompatibile (Teflon, Poliuretano, Silicone) questi possono restare in loco a breve termine 3-4 giorni; o a medio termine fino a 4 settimane.
Per concludere è bene ricordare che la nutrizione parenterale deve essere sospesa gradualmente per consentire l’adattamento dell’assistito a un decremento dei livelli di glucosio.
La Nutrizione Enterale
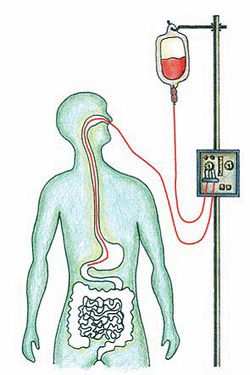
Le diete per la nutrizione enterale. Una miscela nutritiva da somministrare per via enterale deve rispondere innanzitutto al requisito della completezza dovendo contenere tutti i nutrienti indispensabili. Nelle miscele enterali non si opera la distinzione tra le calorie non proteiche e quelle provenienti dall’apporto proteico ma si parla di apporto calorico complessivo. L’apporto calorico totale è suddiviso in una percentuale glucidica del 45-55% , una parte lipidica del 30-35% ed una quota proteica del 12-15% .
Gli oligoelementi, vitamine ed elettroliti sono presenti nelle quantità consigliate dai LARN anche se si è notata una tendenza nelle miscele in commercio ad una concentrazione di vitamine più alta ed un sottodosaggio di elettroliti soprattutto nella loro componente di sodio e potassio, forse per assicurare una migliore tolleranza nei pazienti cardiopatici.
La componente glucidica è rappresentata nella maggior parte dei casi da maltodestrine, talvolta da fruttosio e polimeri del glucosio anche della soia; viene evitato l’impiego del lattosio per il frequente riscontro di intolleranze a tale zucchero. Gli acidi grassi poli-insaturi a provenienza da oli vegetali e lecitina di soia costituiscono la massima parte dei grassi; una quota di trigliceridi a catena media (MCT) viene sempre aggiunta alla quota lipidica, per la caratteristica di queste molecole di diffondere dal sangue senza l’aiuto di alcun meccanismo di trasporto attivo.
La composizione e la quantità di protidi può variare in relazione al tipo di dieta considerata.
Importante è il contenuto in acqua di queste diete che va sempre considerato nella valutazione del bilancio idrico del Paziente; l’acqua libera può variare dall’ 85% delle diete normocaloriche al 60% delle diete ipercaloriche.
Le diete si possono classificare in diete elementari e diete polimeriche.
Le diete elementari contengono nutrienti in forma direttamente o facilmente utilizzabile e sono indicate in tutti quei casi in cui l’intestino presenti grave o completa incapacità digestiva; sono caratterizzate da una elevata osmolarità e sono tutte normocaloriche. Va posta attenzione alla osmolarità alta che può essere alla base di problemi a carico del tratto gastroenterico, tra i quali il più frequente è la diarrea.
Le diete polimeriche sono quelle normalmente utilizzate nella maggior parte dei pazienti; i nutrienti che le costituiscono sono intatti e richiedono quindi una attività digestiva per essere utilizzati. La osmolarità di queste miscele si aggira intorno a valori di 250-350 mOsm/l e contenuto calorico di 1-1,5 kcal/ml. Esistono anche diete in cui la composizione quali-quantitativa varia in relazione a specifiche patologie e situazioni: encefalopatia porto-sistemica, insufficienza respiratoria, diabete, insufficienza renale in trattamento dialitico e non, età pediatrica. Nell’ambito delle diete complete per nutrizione enterale, le diete immunostimolanti sono quelle di più recente introduzione. Esse risultano arricchite di alcuni elementi quali: arginina, glutammina, ribonucleotidi, vitamina E, beta-carotene, zinco e selenio. A dosi superiori a quelle comunemente utilizzate, alcuni tra questi, quali arginina, glutammina ed acidi grassi omega-3 ed omega-6, hanno mostrato evidenza di promuovere azioni benefiche quali una più eclatante attività anabolica proteica o anti-catabolica, stimolare la immuno-competenza, mantenere le funzioni enterocitarie, promuovere la riproduzione di cellule a rapido turnover, migliorare i processi di cicatrizzazione, modulare la risposta citochinica.
Molti dei vantaggi supposti sono stati rilevati in patologie meno impegnative (in paz. post-operati) o in studi selettivi in alcune categorie di pazienti critici. Il razionale accumulato da studi pre-clinici e clinici ha già portato alla commercializzazione di prodotti per N.E. che nella maggioranza dei casi associano più elementi attivi ed il risultato clinico evidenziabile risulta essere un effetto sommatorio o di potenziamento.
La glutammina è un aminoacido che partecipa ad una ampia varietà di processi metabolici e biologici, tra cui l’ammoniogenesi renale, la risposta immune cellulo-mediata, la integrità e la riproduzione enterocitica.
Durante gli stati catabolici la glutamina è mobilizzata in grandi quantità dai tessuti periferici, quali il muscolo scheletrico, e si instaura presto una situazione di bassa disponibilità, tanto che l’aminoacido diviene condizionatamente essenziale. La glutamina protegge l’intestino con triplice meccanismo: innanzitutto è una fonte energetica cellulare, è metabolizzata dai mitocondri con la stessa efficienza del glucosio e può essere particolarmente importante in momenti di stress fisiologico quando l’energia richiesta dagli enterociti è aumentata come in infezioni, trauma, cancro, grandi interventi. In secondo luogo essa è un elemento di base per la costruzione, sintesi dei nucleotidi dal momento che sembra essere l’elemento limitante per la ornitina-decarbossilasi, che è l’enzima chiave per la biosintesi delle pirimidine. Infine il suddetto aminoacido è una sorgente per il glutatione, che è a sua volta un elemento protettivo per l’enterocita e serve come anti-ossidante; la glutamina incrementa il livello di glutatione in tutti i tessuti ed anche dopo somministrazione intestinale il livello risulta più che raddoppiato.
L’arginina, similmente, partecipa alla sintesi dell’urea, alla produzione di ossido nitrico (NO), alla proliferazione e differenziazione linfocitaria, facilita la sintesi di collageno e migliora la cicatrizzazione delle ferite; inoltre induce increzione di GH, prolattina, insulina e somatostatina. Apporti sino a 0,5 g/kg/die si sono associati a evidenze cliniche di migliore risposta immune e resistenza alle infezioni.
Gli acidi grassi poli-insaturi omega-3 sono stati riscontrati di utilità negli stati flogistico-settici in quanto riducono la sintesi di TNF e di ILF-1 promuovendo la sintesi di prostaglandine E3 e leucotrieni B5, mediatori ad azione immuno-competente ed anti-infiammatoria, benefici in questi pazienti critici.
In definitiva, la più elevata concentrazione nella dieta di tali sostanze è stata associata ad un miglioramento della attività immunostimolante con riguardo alla attività anti-citochine e conseguente aumentata resistenza alle complicanze infettive e diminuzione dell’entità della risposta infiammatoria sistemica.
Farmaci procinetici: nel Paziente in N.E. favoriscono la ricomparsa di un’adeguata funzionalità intestinale. La metoclopramide è un agonista dei recettori dopaminergici; agisce soprattutto sul piccolo intestino prossimale e presenta azione di blocco dei recettori dopaminergici; viene somministrata per via parenterale venosa con un dosaggio massimo di 4 fiale/die. Anche il domperidone è un agonista dei recettori dopaminergici che agisce soprattutto sul piccolo intestino prossimale.
Una azione più complessa è alla base della attività procinetica della cisapride; si tratta di una molecola ad attività agonista sui recettori dopaminergici. Incrementa la produzione di acetilcolina endogena e agisce sul tratto intestinale in toto, dall’esofago al colon, aumentando la attività propulsiva e il tono dello sfintere esofageo inferiore. Non possiede azione di blocco dei recettori dopaminergici, ma può presentare interazione con ketoconazolo e suoi derivati, eritromicina e nefazodone, provocando un allungamento dell’intervallo Q-T e facilitando la insorgenza di aritmie e torsioni di punta, per questo da alcuni anni è vietata in Italia. La eritromicina antagonizza la motilina ed ha la sua sede di azione principale nella parte prossimale del piccolo intestino. I fermenti lattici sono molto importanti per ricostituire una flora batterica intestinale equilibrata soprattutto quando il Paziente ha avuto un lungo periodo di digiuno o ha subito un importante e lungo trattamento antibiotico.
Gli oligoelementi, vitamine ed elettroliti sono presenti nelle quantità consigliate dai LARN anche se si è notata una tendenza nelle miscele in commercio ad una concentrazione di vitamine più alta ed un sottodosaggio di elettroliti soprattutto nella loro componente di sodio e potassio, forse per assicurare una migliore tolleranza nei pazienti cardiopatici.
La componente glucidica è rappresentata nella maggior parte dei casi da maltodestrine, talvolta da fruttosio e polimeri del glucosio anche della soia; viene evitato l’impiego del lattosio per il frequente riscontro di intolleranze a tale zucchero. Gli acidi grassi poli-insaturi a provenienza da oli vegetali e lecitina di soia costituiscono la massima parte dei grassi; una quota di trigliceridi a catena media (MCT) viene sempre aggiunta alla quota lipidica, per la caratteristica di queste molecole di diffondere dal sangue senza l’aiuto di alcun meccanismo di trasporto attivo.
La composizione e la quantità di protidi può variare in relazione al tipo di dieta considerata.
Importante è il contenuto in acqua di queste diete che va sempre considerato nella valutazione del bilancio idrico del Paziente; l’acqua libera può variare dall’ 85% delle diete normocaloriche al 60% delle diete ipercaloriche.
Le diete si possono classificare in diete elementari e diete polimeriche.
Le diete elementari contengono nutrienti in forma direttamente o facilmente utilizzabile e sono indicate in tutti quei casi in cui l’intestino presenti grave o completa incapacità digestiva; sono caratterizzate da una elevata osmolarità e sono tutte normocaloriche. Va posta attenzione alla osmolarità alta che può essere alla base di problemi a carico del tratto gastroenterico, tra i quali il più frequente è la diarrea.
Le diete polimeriche sono quelle normalmente utilizzate nella maggior parte dei pazienti; i nutrienti che le costituiscono sono intatti e richiedono quindi una attività digestiva per essere utilizzati. La osmolarità di queste miscele si aggira intorno a valori di 250-350 mOsm/l e contenuto calorico di 1-1,5 kcal/ml. Esistono anche diete in cui la composizione quali-quantitativa varia in relazione a specifiche patologie e situazioni: encefalopatia porto-sistemica, insufficienza respiratoria, diabete, insufficienza renale in trattamento dialitico e non, età pediatrica. Nell’ambito delle diete complete per nutrizione enterale, le diete immunostimolanti sono quelle di più recente introduzione. Esse risultano arricchite di alcuni elementi quali: arginina, glutammina, ribonucleotidi, vitamina E, beta-carotene, zinco e selenio. A dosi superiori a quelle comunemente utilizzate, alcuni tra questi, quali arginina, glutammina ed acidi grassi omega-3 ed omega-6, hanno mostrato evidenza di promuovere azioni benefiche quali una più eclatante attività anabolica proteica o anti-catabolica, stimolare la immuno-competenza, mantenere le funzioni enterocitarie, promuovere la riproduzione di cellule a rapido turnover, migliorare i processi di cicatrizzazione, modulare la risposta citochinica.
Molti dei vantaggi supposti sono stati rilevati in patologie meno impegnative (in paz. post-operati) o in studi selettivi in alcune categorie di pazienti critici. Il razionale accumulato da studi pre-clinici e clinici ha già portato alla commercializzazione di prodotti per N.E. che nella maggioranza dei casi associano più elementi attivi ed il risultato clinico evidenziabile risulta essere un effetto sommatorio o di potenziamento.
La glutammina è un aminoacido che partecipa ad una ampia varietà di processi metabolici e biologici, tra cui l’ammoniogenesi renale, la risposta immune cellulo-mediata, la integrità e la riproduzione enterocitica.
Durante gli stati catabolici la glutamina è mobilizzata in grandi quantità dai tessuti periferici, quali il muscolo scheletrico, e si instaura presto una situazione di bassa disponibilità, tanto che l’aminoacido diviene condizionatamente essenziale. La glutamina protegge l’intestino con triplice meccanismo: innanzitutto è una fonte energetica cellulare, è metabolizzata dai mitocondri con la stessa efficienza del glucosio e può essere particolarmente importante in momenti di stress fisiologico quando l’energia richiesta dagli enterociti è aumentata come in infezioni, trauma, cancro, grandi interventi. In secondo luogo essa è un elemento di base per la costruzione, sintesi dei nucleotidi dal momento che sembra essere l’elemento limitante per la ornitina-decarbossilasi, che è l’enzima chiave per la biosintesi delle pirimidine. Infine il suddetto aminoacido è una sorgente per il glutatione, che è a sua volta un elemento protettivo per l’enterocita e serve come anti-ossidante; la glutamina incrementa il livello di glutatione in tutti i tessuti ed anche dopo somministrazione intestinale il livello risulta più che raddoppiato.
L’arginina, similmente, partecipa alla sintesi dell’urea, alla produzione di ossido nitrico (NO), alla proliferazione e differenziazione linfocitaria, facilita la sintesi di collageno e migliora la cicatrizzazione delle ferite; inoltre induce increzione di GH, prolattina, insulina e somatostatina. Apporti sino a 0,5 g/kg/die si sono associati a evidenze cliniche di migliore risposta immune e resistenza alle infezioni.
Gli acidi grassi poli-insaturi omega-3 sono stati riscontrati di utilità negli stati flogistico-settici in quanto riducono la sintesi di TNF e di ILF-1 promuovendo la sintesi di prostaglandine E3 e leucotrieni B5, mediatori ad azione immuno-competente ed anti-infiammatoria, benefici in questi pazienti critici.
In definitiva, la più elevata concentrazione nella dieta di tali sostanze è stata associata ad un miglioramento della attività immunostimolante con riguardo alla attività anti-citochine e conseguente aumentata resistenza alle complicanze infettive e diminuzione dell’entità della risposta infiammatoria sistemica.
Farmaci procinetici: nel Paziente in N.E. favoriscono la ricomparsa di un’adeguata funzionalità intestinale. La metoclopramide è un agonista dei recettori dopaminergici; agisce soprattutto sul piccolo intestino prossimale e presenta azione di blocco dei recettori dopaminergici; viene somministrata per via parenterale venosa con un dosaggio massimo di 4 fiale/die. Anche il domperidone è un agonista dei recettori dopaminergici che agisce soprattutto sul piccolo intestino prossimale.
Una azione più complessa è alla base della attività procinetica della cisapride; si tratta di una molecola ad attività agonista sui recettori dopaminergici. Incrementa la produzione di acetilcolina endogena e agisce sul tratto intestinale in toto, dall’esofago al colon, aumentando la attività propulsiva e il tono dello sfintere esofageo inferiore. Non possiede azione di blocco dei recettori dopaminergici, ma può presentare interazione con ketoconazolo e suoi derivati, eritromicina e nefazodone, provocando un allungamento dell’intervallo Q-T e facilitando la insorgenza di aritmie e torsioni di punta, per questo da alcuni anni è vietata in Italia. La eritromicina antagonizza la motilina ed ha la sua sede di azione principale nella parte prossimale del piccolo intestino. I fermenti lattici sono molto importanti per ricostituire una flora batterica intestinale equilibrata soprattutto quando il Paziente ha avuto un lungo periodo di digiuno o ha subito un importante e lungo trattamento antibiotico.
La nutrizione parenterale domiciliare (NPD)
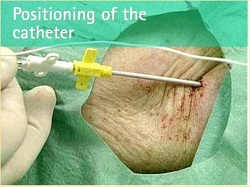
L’N.P.D. permette al paziente che necessita di un supporto nutrizionale, totale o parziale per via venosa, di vivere nel proprio ambiente familiare mantenendo una vita di relazioni sociali ed in taluni casi, di riprendere la propria attività lavorativa.
I primi casi di pazienti in NPD sono stati riportati nella letteratura degli Stati Uniti agli inizi degli anni ’70.
Successivamente questa metodologia si è evoluta con costante miglioramento di materiali, delle formule nutrizionali e dei programmi di gestione necessari per prevenire e limitare le complicanze legate alla nutrizione parenterale protratta.
Indicazioni alla NPD. La somministrazione di nutrienti per via parenterale (NP) è indicata quando la via enterale non è praticabile o quando essa da sola non è in grado di assicurare tutto il fabbisogno calorico-proteico.
Le condizioni cliniche che richiedono una NPD sono:
- fistola digiunale o ileale ad alta portata,
- insufficienza intestinale grave,
- occlusione o sub-occlusione cronica,
- intolleranza alla NE: diarrea, ristagno gastrico, intolleranza alla N.E.,
peritonite.
Nelle IBD (Inflammatory Bowel Diseases) l’indicazione al vero e proprio riposo d’organo è ormai limitata a situazioni cliniche particolari come la presenza di fistole o stati sub-occlusivi.
Nelle patologie neoplastiche, soprattutto con localizzazione al tratto gastro-enterico o successivamente ad interventi chirurgici altamente demolitivi, si tende a limitare la NPD al Paziente libero da tumore o con in atto terapie specifiche.
Vie di accesso per la Nutrizione Parenterale Domiciliare.
I cateteri venosi centrali (C.V.C,) per NPD sono caratterizzati per essere fatti di materiali biocompatibile, silicone o poliuretano, e dalla possibilità di essere tunnellizzati parzialmente sottocute nella porzione prossimale. Sono anche disponibili sistemi totalmente impiantabili forniti sottocute di una membrana perforabile (port-a-cath). Le vie di accesso si possono classificare in base alla regione di introduzione ed al tempo di permanenza in:
- cateterismo venoso periferico (tipo Drumm) e cateterismo venoso centrale,
- venipuntura periferica (PICC) e venipuntura centrale (v.succlavia e v.giugulare interna).
Accessi venosi a lungo termine:
- sistemi esterni tunnellizzati e
- sistemi totalmente impiantabili tipo Port.
Le complicanze più gravi dell’accesso vascolare sono la sepsi e la trombosi dei grossi vasi che richiedono la rimozione del catetere venoso o il trattamento in regime di ricovero.
AVVERTENZA: Questo sito ha carattere di divulgazione culturale e informativa, necessariamente generale. Le informazioni contenute, pur basate sugli studi scientifici citati, non sostituiscono il consulto personalizzato del professionista pratico, dietologo o medico. Il lettore non è autorizzato a considerare gli articoli qui contenuti come consulti medici, né a prenderli a pretesto per curarsi da sé.
I primi casi di pazienti in NPD sono stati riportati nella letteratura degli Stati Uniti agli inizi degli anni ’70.
Successivamente questa metodologia si è evoluta con costante miglioramento di materiali, delle formule nutrizionali e dei programmi di gestione necessari per prevenire e limitare le complicanze legate alla nutrizione parenterale protratta.
Indicazioni alla NPD. La somministrazione di nutrienti per via parenterale (NP) è indicata quando la via enterale non è praticabile o quando essa da sola non è in grado di assicurare tutto il fabbisogno calorico-proteico.
Le condizioni cliniche che richiedono una NPD sono:
- fistola digiunale o ileale ad alta portata,
- insufficienza intestinale grave,
- occlusione o sub-occlusione cronica,
- intolleranza alla NE: diarrea, ristagno gastrico, intolleranza alla N.E.,
peritonite.
Nelle IBD (Inflammatory Bowel Diseases) l’indicazione al vero e proprio riposo d’organo è ormai limitata a situazioni cliniche particolari come la presenza di fistole o stati sub-occlusivi.
Nelle patologie neoplastiche, soprattutto con localizzazione al tratto gastro-enterico o successivamente ad interventi chirurgici altamente demolitivi, si tende a limitare la NPD al Paziente libero da tumore o con in atto terapie specifiche.
Vie di accesso per la Nutrizione Parenterale Domiciliare.
I cateteri venosi centrali (C.V.C,) per NPD sono caratterizzati per essere fatti di materiali biocompatibile, silicone o poliuretano, e dalla possibilità di essere tunnellizzati parzialmente sottocute nella porzione prossimale. Sono anche disponibili sistemi totalmente impiantabili forniti sottocute di una membrana perforabile (port-a-cath). Le vie di accesso si possono classificare in base alla regione di introduzione ed al tempo di permanenza in:
- cateterismo venoso periferico (tipo Drumm) e cateterismo venoso centrale,
- venipuntura periferica (PICC) e venipuntura centrale (v.succlavia e v.giugulare interna).
Accessi venosi a lungo termine:
- sistemi esterni tunnellizzati e
- sistemi totalmente impiantabili tipo Port.
Le complicanze più gravi dell’accesso vascolare sono la sepsi e la trombosi dei grossi vasi che richiedono la rimozione del catetere venoso o il trattamento in regime di ricovero.
AVVERTENZA: Questo sito ha carattere di divulgazione culturale e informativa, necessariamente generale. Le informazioni contenute, pur basate sugli studi scientifici citati, non sostituiscono il consulto personalizzato del professionista pratico, dietologo o medico. Il lettore non è autorizzato a considerare gli articoli qui contenuti come consulti medici, né a prenderli a pretesto per curarsi da sé.

